© Copyright 2023 [沈阳朗云志雅科技有限公司]
地址:沈阳市沈河区团结路11号金融中心A1座3201 邮箱:service@sylyzy.com
技术服务咨询:13898168872 项目申报咨询:13504002441
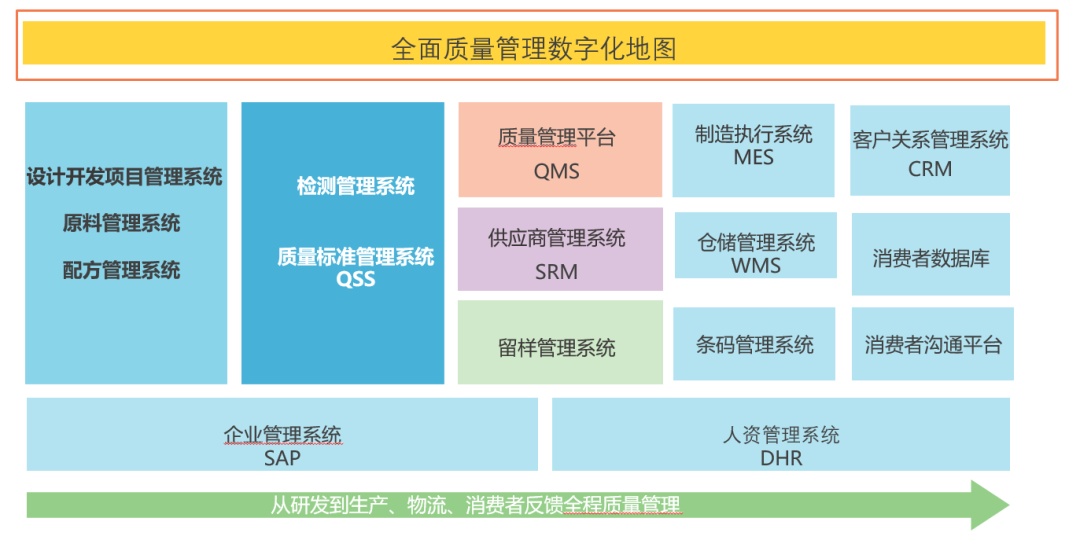
1.功能模块:依据GMP法规要求专为制药企业设计的数字化质量管理平台,支持质量管理的合规性和数据完整性的管理系统。涵盖文件管理、培训管理、变更管理、客户投诉管理、偏差CAPA管理、供应商管理、药品召回管理、不良反应管理、风险评估管理、自检管理、验证管理、QMS台账、基础管理等功能模块。
2.价值作用:大幅度提升企业质量事件处理效率和准确性,满足国内外法规审计需求,为管理层质量决策提供依据。
3.在制药行业,质量是企业的生命线。为了满足严格的 GMP 法规要求,提升质量管理水平,我们推出了专为制药企业设计的数字化质量管理平台。
一、功能模块
(一)文件管理
1. 对各类质量文件进行分类、编号和存储,确保文件的准确性和可追溯性。
2. 实现文件的起草、审核、批准和分发的电子化流程,提高文件管理效率。
(二)培训管理
1. 制定详细的培训计划,包括培训课程、培训对象和培训时间。
2. 记录员工的培训参与情况和考核结果,确保员工具备相应的质量知识和技能。
(三)变更管理
1. 对生产工艺、设备、原材料等方面的变更进行严格控制和审批。
2. 评估变更对产品质量的潜在影响,确保变更的合理性和安全性。
(四)客户投诉管理
1. 及时接收和记录客户的投诉信息,包括投诉内容、投诉产品批次等。
2. 对投诉进行调查和处理,采取相应的纠正措施,并向客户反馈处理结果。
(五)偏差 CAPA 管理
1. 识别和记录生产过程中的偏差事件,分析偏差产生的原因。
2. 制定并实施纠正和预防措施(CAPA),跟踪措施的执行效果,防止偏差再次发生。
(六)供应商管理
1. 对供应商进行资质审核和评估,建立供应商档案。
2. 监控供应商的供货质量和服务表现,及时处理供应商相关的质量问题。
(七)药品召回管理
1. 制定药品召回计划和流程,确保在需要召回药品时能够迅速、有效地执行。
2. 记录召回药品的信息和处理情况,向监管部门报告召回进展。
(八)不良反应管理
1. 收集和分析药品不良反应信息,及时上报监管部门。
2. 评估不良反应的严重程度和潜在风险,采取相应的风险管理措施。
(九)风险评估管理
1. 运用风险评估工具和方法,对生产过程、产品质量等方面的风险进行识别和评估。
2. 根据风险评估结果制定相应的控制措施,降低风险水平。
(十)自检管理
1. 制定自检计划和检查表,定期对质量管理体系进行内部检查。
2. 记录自检发现的问题,制定整改措施并跟踪整改效果。
(十一)验证管理
1. 对生产工艺、设备、清洁方法等进行验证,确保其符合预定的要求。
2. 管理验证方案、报告和数据,保证验证过程的合规性和有效性。
(十二)QMS 台账
1. 建立质量管理相关的各类台账,如质量指标台账、不合格品台账等。
2. 对台账数据进行统计分析,为质量管理决策提供数据支持。
(十三)基础管理
1. 包括用户管理、权限设置、系统配置等基础功能,确保系统的安全稳定运行。
2. 提供系统操作指南和帮助文档,方便用户使用。
二、价值作用
(一)提升效率和准确性
1. 自动化质量管理流程,减少人工操作和纸质文件的流转,大大提高工作效率。
2. 系统的标准化和规范化操作,降低人为错误的发生概率,提高质量事件处理的准确性。
(二)满足法规审计需求
1. 严格遵循 GMP 法规要求设计,确保质量管理活动的合规性。
2. 提供完整、准确的质量管理数据和记录,轻松应对国内外法规审计。
(三)支持决策
1. 实时数据分析和报表生成,为管理层提供全面、及时的质量信息。
2. 帮助管理层准确把握质量状况,制定科学合理的质量决策,提升企业质量管理水平。
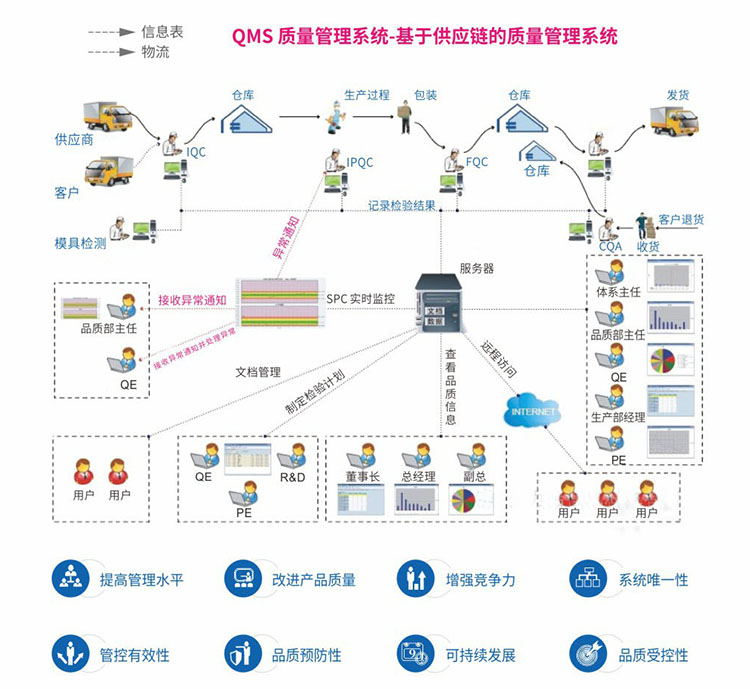
通过引入我们的数字化质量管理系统(QMS),制药企业能够实现质量管理的数字化、标准化和智能化,大幅度提升质量管理效能,保障药品质量安全,增强企业的市场竞争力。
© Copyright 2023 [沈阳朗云志雅科技有限公司]
地址:沈阳市沈河区团结路11号金融中心A1座3201 邮箱:service@sylyzy.com
技术服务咨询:13898168872 项目申报咨询:13504002441
